学术资源
一例由转座子插入导致的耳聋病例
一、患者基本信息
▶ 性别:女
▶ 年龄:34岁
▶ 样本类型:外周血
▶ 临床诊断:本人听力差,母亲听力不好,家族中有耳聋的孩子
▶ 检测项目:OmniSeek®全外显子组检测

二、检测结果
① 检测结果分析及验证
OmniSeek®全外显子组检测常规SNV和CNV分析结果均为阴性;利用金诺诊断自主开发的基于WES数据移动元件插入变异(Mobile element insertion, MEI)生信分析流程进一步分析发现,该受检者POU4F3基因的第2号外显子上可能插入了Alu元件(图1)。进一步序列分析提示插入Alu元件,Sanger测序验证结果和PCR扩增+凝胶电泳分析与NGS结果相吻合(图2和图3)。
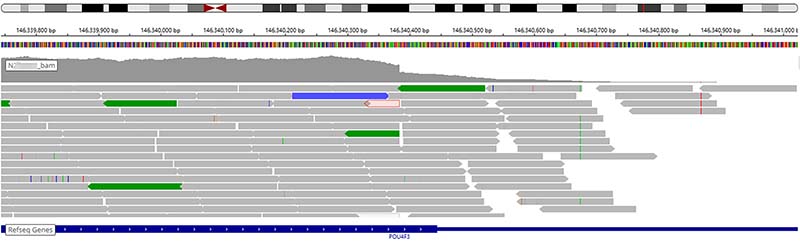
图1.受检者POU4F3基因c.9**_9**insAlu变异 测序结果IGV示意图
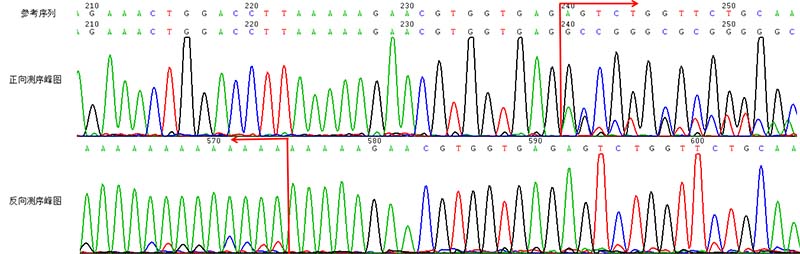
图2.受检者POU4F3基因c.9**_9**insAlu变异 Sanger测序验证结果示意图
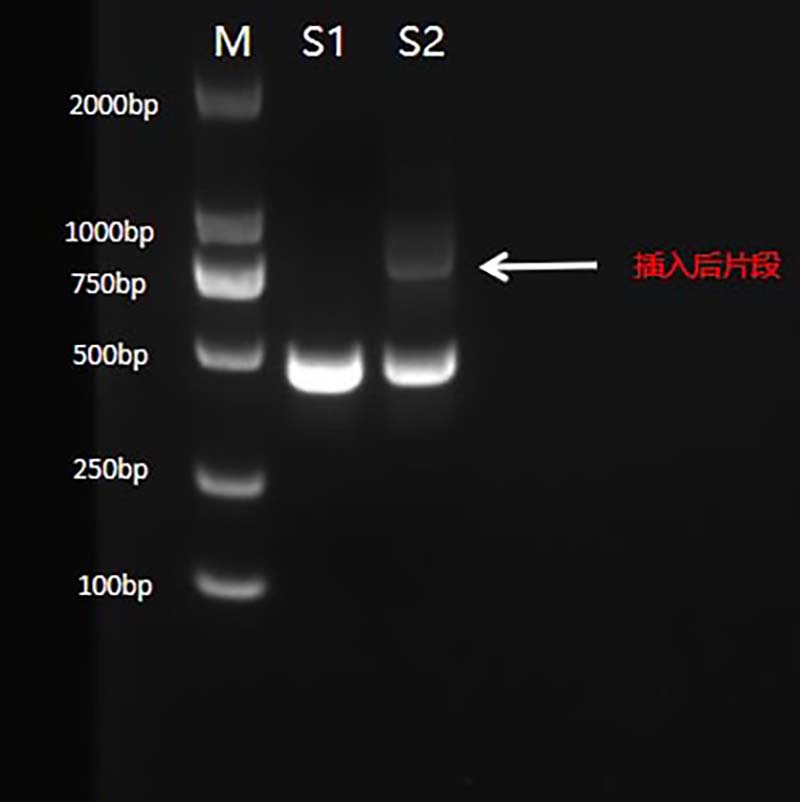
图3.受检者POU4F3基因c.9**_9**insAlu变异 PCR结果示意图。M.DL2000 maker;S1.阴性对照;S2.受检者;→为插入位置。
② 检测结果解读
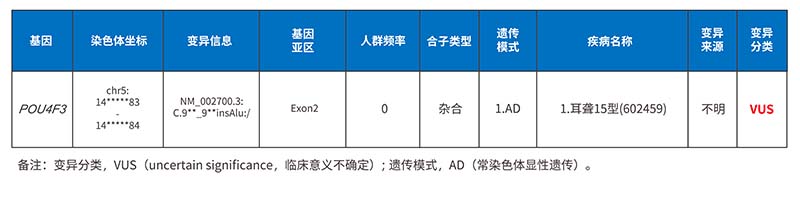
POU4F3: NM_002700.3:exon2:c.956_957insAlu:/:临床意义不确定的变异(PM2_Supporting+PVS1_Moderate)
POU4F3基因位于染色体5q32。人类孟德尔遗传学(OMIM)数据库中记载,POU4F3基因的致病性变异可导致呈常染色体显性遗传的耳聋15型(Deafness, autosomal dominant 15, DFNA15)。DFNA15是一种进行性非综合征型感音神经性耳聋,听力损失是渐进性的,通常在20~60岁发病(OMIM, https://www.omim.org/entry/602459)。
经检测和分析,在受检者POU4F3基因中检测到c.956_957insAlu,即c.956和c.957之间插入了Alu元件。Alu家族是人类基因组中含量最高、活性最强的逆转录转座子。Alu元件是短散在重复序列SINE家族的成员,大小约300bp,包括polyA尾和靶位点复制序列[1-2]。本次检测到的Alu元件插入在外显子区,推测该变异可能为功能缺失性变异(LoF),已知LoF是POU4F3基因相关疾病的致病机制(ClinGen HI 值=3),该变异位于第2号外显子(共2个外显子),预计导致<10%蛋白序列丢失,且该外显子位于生物学相关转录本中。GnomAD数据库全外显子组数据集和全基因组数据集均未收录该变异。该变异尚无文献报道。
结合上述检测结果,受检者检出的POU4F3基因第2号外显子Alu元件插入,符合耳聋15型的遗传模式,支持受检者听力差的临床表型及受检者母亲听力不好、家族中有耳聋的孩子的家族史。
三、转座子插入变异与单基因遗传病
移动元件(Mobile elements, ME)或转座元件(Transposable elements, TE)几乎占据了人类基因组的一半,是散布在真核生物基因组中的重复基因序列,通过其独有的序列和编码的转座酶,可以在基因组中复制自身到不同位置,故又称为转座子或跳跃基因。转座子可根据转座机制的不同分为两大类(图4)[3]:
1)DNA转座子,占基因组的3-5%,在人类基因组中是不可移动的。
2)逆转录转座子,是人类中唯一活跃的TE。一个活跃的TE有可能在基因组内移动到新的位置,插入到原始DNA序列中。根据是否存在长末端重复序列(LTR)又分为两类,逆转录转座子又分为:a)LTR逆转录转座子/人类内源性逆转录病毒(HERV):长10Kb(但截短元件相对常见),约占人类基因组的8%,并以孟德尔遗传方式传给后代。HERV在产前尤其活跃,可能影响神经发育。证据支持许多HERV的长末端重复(LTR)区域包含转录因子的结合位点。这些启动子可以激活HERV或位于LTR下游的其他基因。HERV的特点是移动活动非常有限,尽管某些元素可能保留了通过逆转录病毒样机制移动的能力。b)非LTR逆转录转座子,这些转座子包括长插入元件(LINE,占基因组的20.4%)、短插入元件(SINEs,10.2%)和SVA(SINE-R/VNTR/Alu-like,2.6%)。
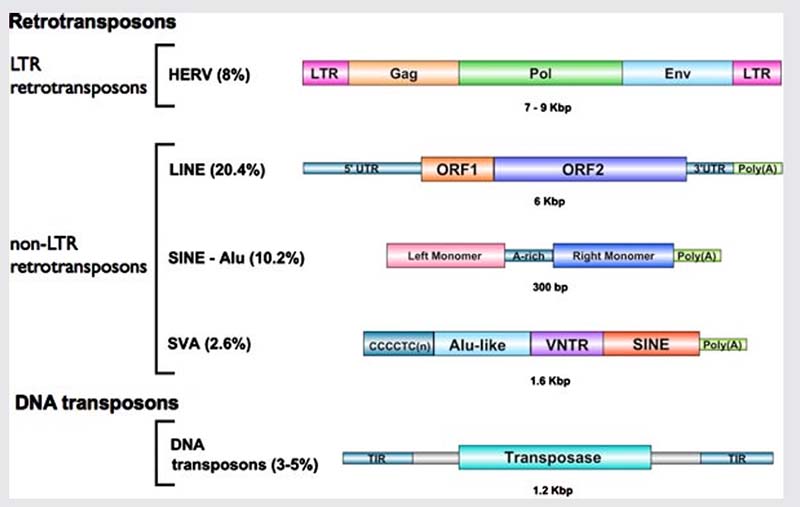
图4.转座因子的分类和分子结构。注:a)LTR转座子/人类内源性逆转录病毒(HERV):分类为30-50个不同的家族,结构上类似于外源性逆转录病毒,具有两个长末端重复序列,位于功能性多蛋白衣壳(gag)、蛋白酶、聚合酶和逆转录酶(pol)和包膜(env)的编码序列两侧,但缺乏离开细胞所需的包膜成分;b)LINE有三个主要家族,L1、L2和L3,但只有L1家族通过复制和粘贴机制(一种称为直接逆转录转座(RT)的过程)使用RNA中间体在人类基因组中保持转座能力。L1元件需要完整的50个非翻译区(UTR)作为内部启动子,并产生含有功能性ORF1(开放阅读框)和ORF2蛋白的全长L1 mRNA,编码逆转录酶;c)SINE-Alu元件由一个代表内部启动子伸展的tRNA相关区域组成,后面是一个tRNA无关区域和一条线相关区域,被SINE元件用来结合LINE编码的蛋白质以完成LINE-1介导的反转座;d)SVA由四个结构域组成,包括50末端富含CT的重复序列,通常称为CT-六聚体。Alu样序列,与两个反义Alu样片段同源,一种GC可变数目串联重复序列(VNTR),其长度确定全长SVA元件的变异,该元件是一种来自包膜基因(env)的序列;e)DNA转座子:一种称为转座酶(transposase)的蛋白质与侧翼的末端反向重复序列(TIRs)结合TE从供体位置切除TE并将其重新整合到基因组中。
已有文献报道,在神经精神疾病(如精神分裂症、双相情感障碍、重度抑郁症等)病例中报告过TE(图5)[3]。TE在听力异常的病例中极少报道,曾在临床表型包含感音神经性耳聋的X连锁无丙种球蛋白血症(XLA)患者中发现BTK基因中存在Alu元件插入[4]。
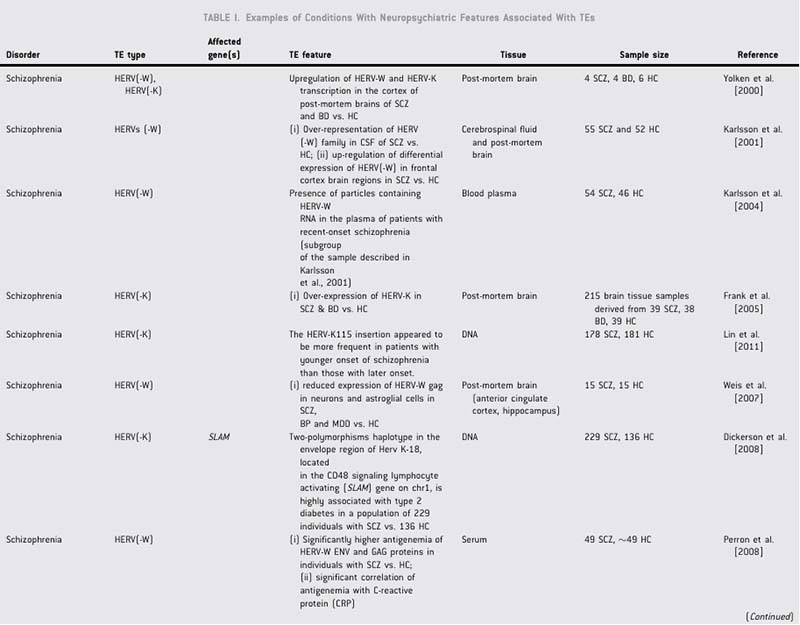
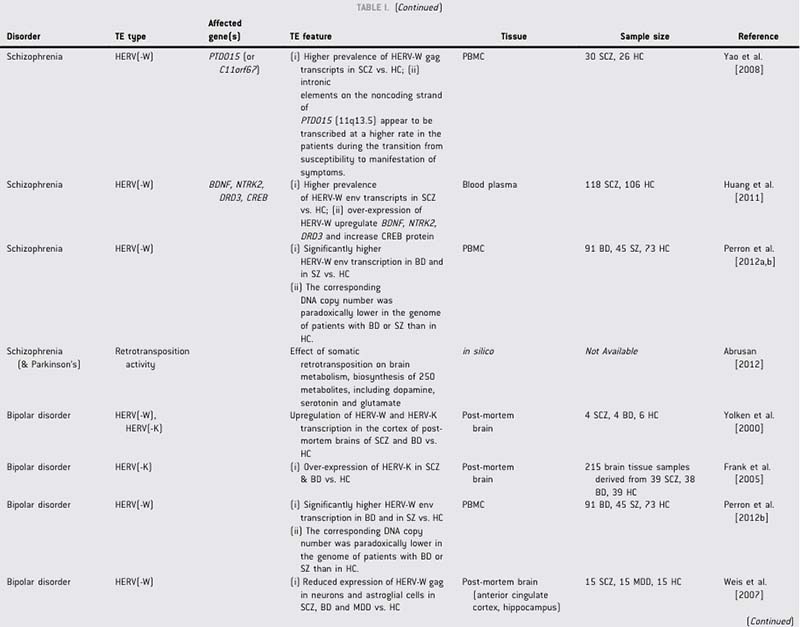
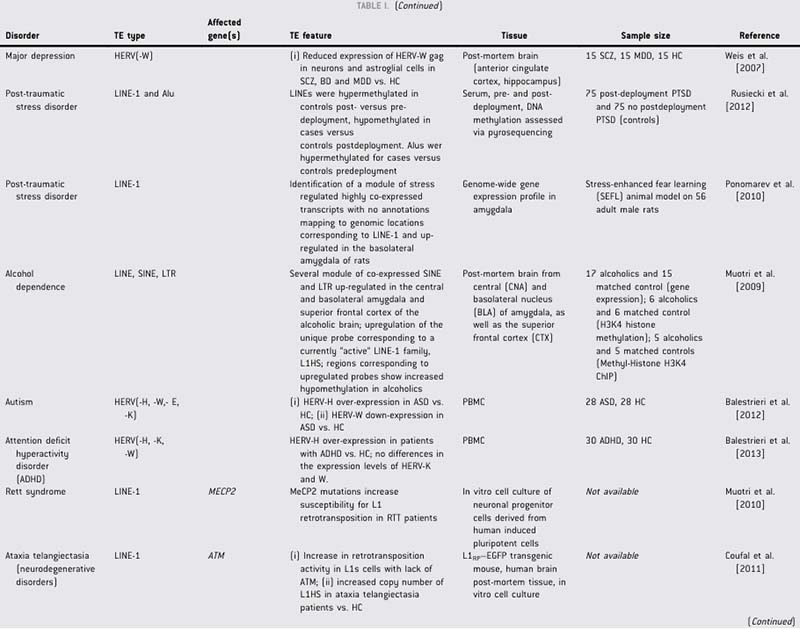
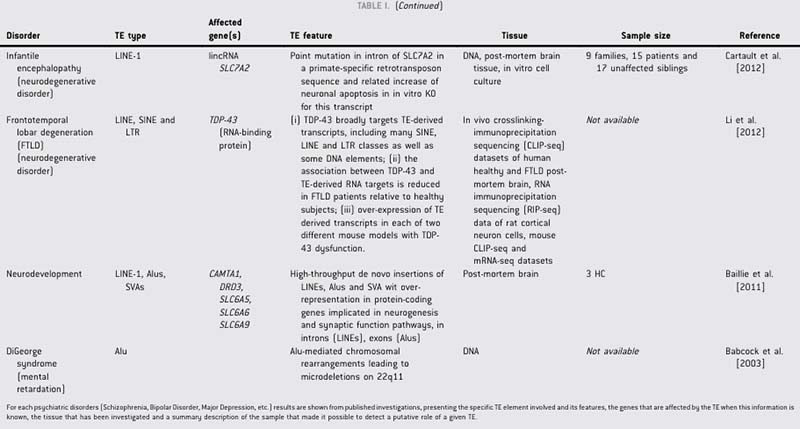
图5.神经精神疾病病例中的转座子
四、结论
转座子插入变异是一种比较罕见的单基因遗传病的发病机制,当常规的SNV和CNV分析为阴性且表型和家族史高度怀疑某种或某类单基因遗传病时,应额外关注转座子的分析结果。
参考文献
1. Genome Biol Evol . 2015 Aug 29;7(9):2608-22.[PMID: 26319576]
2. Mob DNA . 2017 Jul 27:8:9. [PMID: 28770012]
3. Am J Med Genet B Neuropsychiatr Genet. 2014 Apr;165B(3):201-16.[PMID: 24585726]
4. J Hum Genet. 2011 Aug;56(8):577-82.[ PMID: 21753765]
