学术资源
鸟样面容就一定是鸟面综合征么?
前言
去年曾写过一篇关于鸟面综合征(TCS)的病例报道,当看到患者照片(从正面和侧面拍)时,特别明显的小下颌和下颌后缩,心想该不会又是一例鸟面综合征患者吧,但患者还存在右腿髋关节发育不良和皮肤异常,想来可能是由两种不同疾病所致。虽然未猜中开头,但幸运地猜中了结局,还是挺有意思的,一起来看下吧!
受检者基本信息
· 性别:女
· 年龄:3岁
· 样本类型:外周血
· 临床诊断:特殊面容,小下颌;右腿髋关节发育不良?颈部及腿部散在性牛奶咖啡斑;身高:96cm;体重:15.5kg;家属述其智力及语言发育尚可(受检者照片涉及隐私,不便上传)
· 检测项目:OmniSeek®核心家系全外显子组检测
检测结果
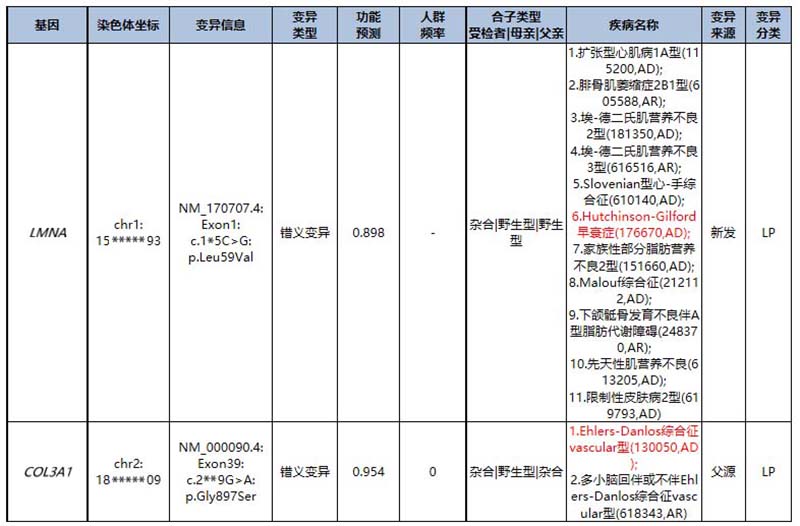
① LMNA:NM_170707.4:Exon1:c.1*5C>G:p.Leu59Val:可能致病性变异(PM2_Supporting+PP3_Moderate+PP2+PS4_Supporting+PS2_Moderate+PP4)
▶ 评级证据
a. PM2_Supporting:gnomAD数据库和本地数据库均未收录该变异。
b. PP3_Moderate:REVEL功能预测软件结果偏向于致病性变异,预测值为0.898,预测结果仅供参考。
c. PP2:LMNA基因的Z值为3.1(≥3.09),错义变异是导致LMNA基因相关疾病的常见机制。
d. PS4_Supporting+PS2_Moderate:仅少数文献报道在1例临床表型为非典型早衰综合征和心肌病的患者中检测到LMNA基因变异c.1*5C>G,且为新发变异(de novo)[1]。本例受检样本也检测到该变异,且为新发变异(de novo)。
e. PP4:该受检者的临床症状符合HGPS的主要表型。
▶ 其他相关信息
a. 疾病数据库报道:该变异收录于HGMD数据库(CM1515643),ClinVar数据库未收录该变异。
LMNA基因位于染色体1q22。人类孟德尔遗传学(OMIM)数据库中记载,LMNA基因的致病性变异可导致常染色体显性遗传的Hutchinson-Gilford早衰症(Hutchinson-Gilford progeria,HGPS)和常染色体隐性遗传的下颌骨末端发育不良伴A型脂肪代谢障碍(Mandibuloacral dysplasia with type A lipodystrophy,MADA)等多种疾病。
其中,MADA患者主要临床表型包括生长迟缓、颅面异常(如下颌骨发育不全、鸟样面容、脸颊丰满、眼睛突出、尖鼻、喙鼻、高弓形腭、无舌、牙齿过度拥挤/脱落发育不良)、锁骨发育不全、远端指骨和锁骨进行性骨质溶解、皮肤异常(如斑驳病、皮肤萎缩(尤其是手和脚)、软组织钙质沉着症)、脱发以及脂肪代谢障碍(脂肪组织明显肢端丢失,颈部和躯干脂肪组织正常或增加)。胰岛素抵抗和糖尿病可导致代谢并发症。该病通常在儿童期发病。(OMIM,https://omim.org/entry/248370)
HGPS患者主要临床表型包括特征性面容(如颅面不对称、小颌畸形、下颌后缩、眉毛稀疏、睫毛稀疏、鼻梁狭窄、宽鼻尖、舌系带过短、尖颚、牙齿萌出延迟、牙髓发育不良、牙齿拥挤)、脂肪代谢障碍、脱发、指甲营养不良、皮肤异常(如硬皮病、皮肤斑点、皮肤色素沉着过度、皮肤色素减退)、心血管异常(如心绞痛、心肌梗死、早发动脉粥样硬化)和骨骼异常(如髋关节脱位/外翻、远端指骨的肢端骨溶解、锁骨短、梨形胸部)等,运动和智力发育正常。大多数患者临床诊断的中位年龄为19个月,心血管损害可能导致过早死亡。经典型HGPS患者通常携带致病性变异c.1**4C>T(约90%的HGPS),而非经典型HGPS患者诊断时年龄较晚。该病多由LMNA基因新发变异(de novo)所致。(OMIM,https://omim.org/entry/176670,https://www.ncbi.nlm.nih.gov/books/NBK1121/)
MADA和HGPS临床表型存在重叠包括特征性面容(如下颌骨发育不全、小颌畸形、下颌后缩)、脂肪代谢障碍、皮肤异常、脱发、远端指骨的肢端骨溶解等,HGPS患者还可能存在髋关节脱位/外翻的临床表征。此外,HGPS多由LMNA基因新发变异(de novo)所致。本例受检样本和文献报道在1例临床表型为非典型早衰综合征和心肌病的患者中检测到LMNA基因变异c.1*5C>G,均为新发变异(de novo)[1]。由此,将疾病锁定到常染色体显性遗传的HGPS。
②COL3A1:NM_000090.4:Exon39:c.2**9G>A:p.Gly897Ser:可能致病性变异
(PM2_Supporting+PP3_Strong+PP2+PS4_Supporting)
▶ 评级证据
a. PM2_Supporting:gnomAD数据库全外显子组数据集显示该变异在总体人群中的频率为6.847e-7,在东亚人群中的频率为0;gnomAD数据库全基因组数据集显示该变异在总体人群中的频率为6.581e-6,在东亚人群中的频率为0。本地数据库未收录该变异。
b. PP3_Strong:REVEL功能预测软件结果偏向于致病性变异,预测值为0.954,预测结果仅供参考。
c. PP2:COL3A1基因的Z值为4.61(≥3.09),错义变异是导致COL3A1基因相关疾病的常见机制。
d. PS4_Supporting:已有文献报道在至少2例EDSVASC患者中检测到COL3A1基因变异c.2**9G>A[2-3]。
▶ 其他相关信息
a. 疾病数据库报道:HGMD数据库未收录该变异,ClinVar数据库报道该变异为致病性变异/可能致病性变异(2颗星)。
b. 变异来源:经父母样本验证,受检样本COL3A1基因变异c.2**9G>A遗传自父亲,父亲相关表型未知。
COL3A1基因位于染色体2q32.2。人类孟德尔遗传学(OMIM)数据库中记载,COL3A1基因的致病性变异可导致常染色体显性遗传的血管型Ehlers-Danlos综合征(Ehlers-Danlos syndrome, vascular type,EDSVASC)和常染色体隐性遗传的多小脑回伴或不伴血管型Ehlers-Danlos综合征(Polymicrogyria with orvwithout vascular-type EDS,PMGEDSV)。
其中,EDSVASC患者主要特征是以妊娠期动脉和肠破裂,以及子宫破裂为并发症,常见的临床表型包括特殊面容(小颌畸形、薄唇、圆锥形角膜、鼻子狭窄等)、牙齿过早脱落、容易瘀伤、皮肤薄并可见明显的静脉等,其他临床症状包括关节过度活动(主要表现在手指)和皮肤过度伸展(很少或不存在)等。部分患者还可能存在远端关节过度活动、先天性髋关节脱位、马蹄内翻足等临床表型。大多数患者是通过重大并发症确诊的,平均年龄约为30岁。(OMIM,https://www.omim.org/entry/130050)
PMGEDSV患者的临床表型高度可变,主要临床表型包括多小回和其他可变脑结构异常,部分患者有发育迟缓、癫痫发作和面容异常(如闷闷不乐脸、下颌后缩、小颌畸形、平滑/短人中、眼睛深陷、眼球运动异常、夹紧状鼻、薄唇)等。此外,部分患者还可能存在缔组织缺陷(如小关节过度活动、皮肤薄而半透明、易瘀伤、静脉曲张、血管脆性、动脉瘤、主动脉夹层、血管夹层)。该病通常在儿童早期发病,患者可能会因血管夹层而过早死亡。(OMIM,https://www.omim.org/entry/618343)
COL3A1基因相关的EDSVASC患者也存在“小颌畸形、先天性髋关节脱位”的临床表征,已有文献报道在至少2例EDSVASC患者中检测到COL3A1基因变异c.2**9G>A[2-3]。该变异遗传自父亲,父亲相关临床表型未知。但EDSVASC临床不易诊断,大多数患者是通过重大并发症确诊的,平均年龄约为30岁。建议进一步评估父亲的临床表型。
③受检者及其父母测序结果示意图
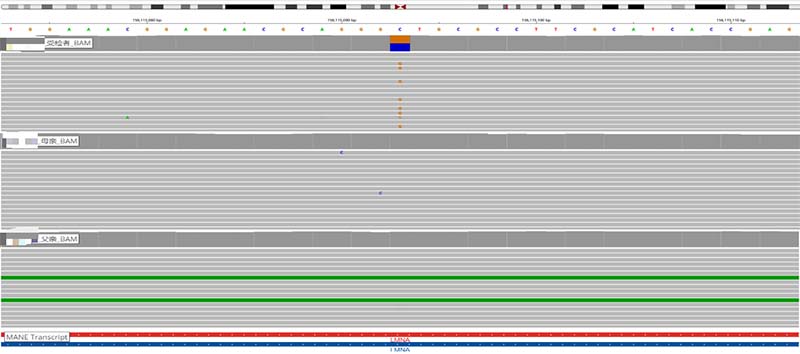
图1.受检者及其父母LMNA基因变异c.1*5C>G 测序结果IGV示意图
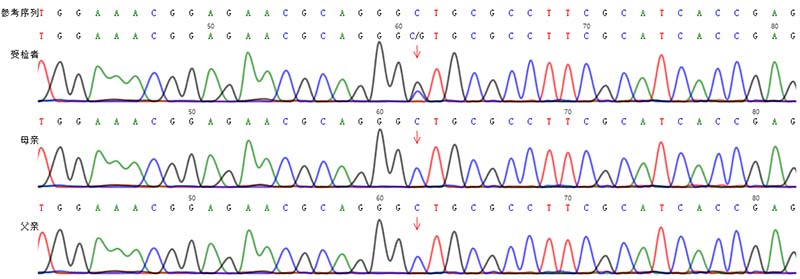
图2.受检者及其父母LMNA基因变异c.1*5C>G Sanger验证结果示意图
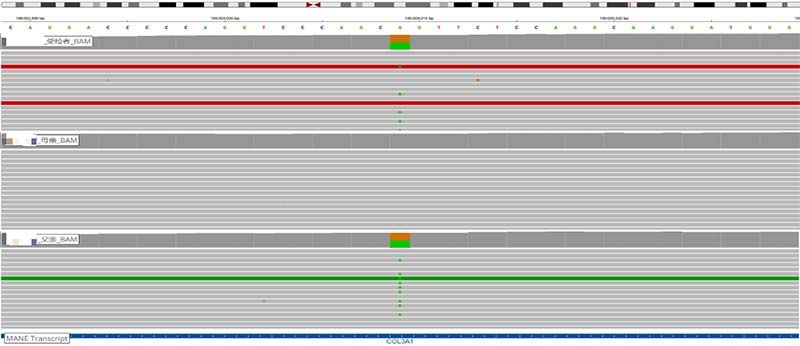
图3.受检者及其父母COL3A1基因变异c.2**9G>A 测序结果IGV示意图
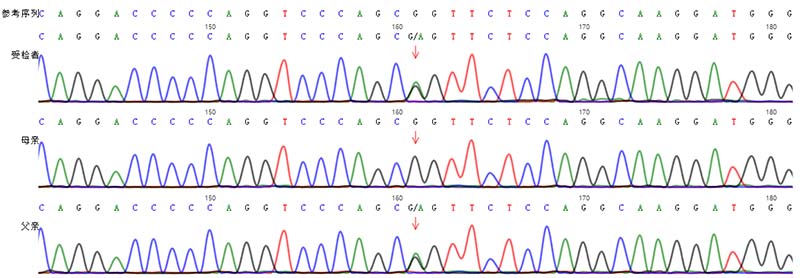
图4.受检者及其父母COL3A1基因变异c.2**9G>A Sanger验证结果示意图
思考与总结
一、同一基因可能对应临床表型存在重叠但遗传模式不同的多种疾病,需要综合患者表型、疾病致病机制和文献病例等因素,去明确基因变异到底与哪种疾病相关。
二、对于病情较为复杂的患者,可考虑由多种疾病叠加导致的结果。在找到一个与受检者临床表型相关的(可能)致病性变异的情况下,不要漏掉其他与受检者临床表型相关的符合遗传模式的(可能)致病性变异。
三、FDA于2020年11月20日批准Eiger生物制药公司(Eiger BioPharmaceuticals, Inc.)的新药Zokinvy(lonafarnib,洛那法尼,CAS登记号为193275⁃84⁃2)胶囊用于治疗HGPS和其他某些特定早老样核纤层蛋白病(Progeroid Laminopathies)。Zokinvy主要用于减少HGPS患者的死亡风险,也可用于1岁及以上的儿童患者治疗某些早老样核纤层蛋白病。用药患者须进行定期血液常规检查和眼部检查。但受检者兼并2种疾病,在治疗方面需要遵循临床医嘱进行决策。
参考文献
1.Can J Cardiol. 2016 Sep;32(9):1166.e29-31. [PMID:27265359]
2.Am J Med Genet A. 2022 Sep;188(9):2777-2782. [PMID:35543214]
3.Clin Genet. 2022 Sep;102(3):191-200. [PMID:35699227]
