学术资源
一例SNV+外显子水平杂合缺失的肌营养不良病例
受检者基本信息
•受检者:男
•年龄:30岁
•主诉:双下肢肌萎缩2年余
•临床病史:患者于2+年前自觉双下肢无力,伴肌萎缩,无肌肉痛,无肌肉跳动,曾于***医院化验肌酶6752U/L,行肌电图检查提示"双胫前肌中等自发电位",骨骼肌病理结果提示进行性肌营养不良,符合dysferlinopathy,提示肢带型肌营养不良2B型诊断。
---------------------------------------------------------------------------------------------------------------
根据肌肉活检提示肢带型肌营养不良2B型,受检者进一步进行了基因检测,选择***公司的肌肉病Panel检测项目。检测报告显示"未发现临床表型高度相关且致病性证据充分的基因变异",即未发现可以解释受检者表型的变异。报告附录中提示的可疑变异包括ATP1A1基因变异c.3**5G>A、DYSF基因变异c.1**4G>T和ITGA7基因变异c.4**G>A。
患者病情仍进行性加重,逐渐累及双下肢近端,蹲起及上下楼费力。再次求诊,门诊以"肌萎缩"收入院。入院主症:双下肢肌萎无力,远端为主,勾脚及踮脚费力,蹲起及上下楼费力。
根据临床信息和检查结果,仍高度怀疑“肌营养不良?”故送检我司OmniSeek®全外显子组检测项目,想进一步排查是否有遗漏。
---------------------------------------------------------------------------------------------------------------
分析结果及验证
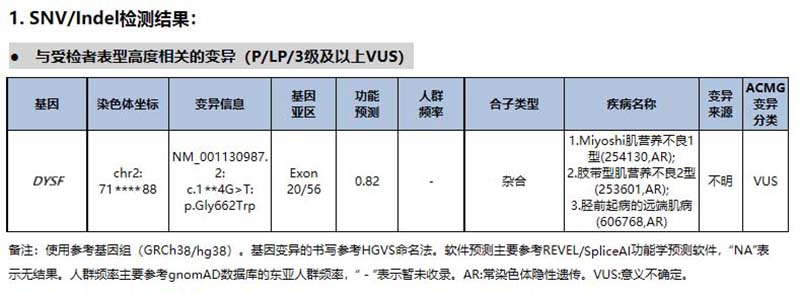
主要分析策略:根据受检者提供的临床信息,进行表型驱动分析。初步分析后,在SNV/Indel结果中发现受检者检出了其他公司附录报告的3个变异(见图1)。
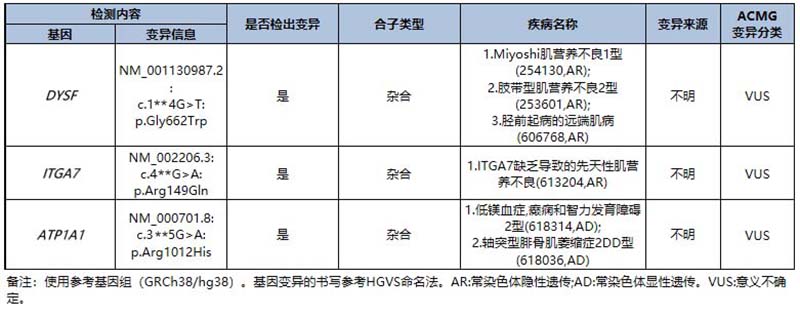
图1.与受检者临床表型部分相关的变异
其中,DYSF基因和ATGA7基因相关的疾病均为常染色体隐性遗传疾病,受检者均检出上述基因的一个杂合变异,无法解释表型。而ATP1A1基因虽然与常染色体显性遗传病相关,遗传模式相符,但ATP1A1基因变异c.3**5G>A的致病性证据不足,属于VUS-low,不能做为临床诊断的依据。
由于临床高度怀疑“肌营养不良?”那是否DYSF基因或ATGA7基因存在另一个被遗漏的变异呢?
根据人类孟德尔遗传学(OMIM)数据库中记载,ATGA7基因相关的ITGA7缺乏导致的先天性肌营养不良主要在婴儿期发病,与患者的发病年龄不符,故暂时排除。DYSF基因的致病性变异可导致肢带型肌营养不良2型(Muscular dystrophy, limb-girdle, 2, LGMDR2)、Miyoshi肌营养不良1型(Miyoshi muscular dystrophy 1, MMD1)以及胫前起病远端型肌病(Myopathy, distal, with anterior tibial onset, DMAT)。上述疾病均呈常染色体隐性遗传模式,且通常在成年早期发病。
① Miyoshi肌营养不良1型
MMD1患者主要表现为远端肌无力和肌萎缩,且上肢和下肢同时受累,但保留了手部固有肌肉,脚尖站立受损,爬楼梯困难,行走困难,但通常仍可活动,血清肌酸激酶升高,肌肉活检显示肌病和营养不良的变化与坏死。
OMIM,https://www.omim.org/entry/254130
② 肢带型肌营养不良2型
LGMDR2(过去也被称为LGMD2B)患者的主要临床表型为近端肌无力,主要累及下肢,上肢受累较晚或根本没有受累,肌电图显示肌病改变,血清肌酸激酶升高,肌肉活检显示肌病和营养不良的变化与坏死。
OMIM,https://www.omim.org/entry/253601
③胫前起病远端型肌病
DMAT患者主要表现为肌肉活检显示肌病且无空泡,首先累及胫骨前肌,血清肌酸激酶升高。
OMIM,https://www.omim.org/entry/606768
从发病年龄和表型角度考虑,DYSF基因的相关度较高。
---------------------------------------------------------------------------------------------------------------
另一方面,目前已发现的DYSF基因变异c.1**4G>T具有一定证据支持其致病性(包括人群频率罕见且REVEL功能预测软件结果偏向于致病)。因此,我们将后续深度挖掘的重点放在了DYSF基因上。
惊喜的是,通过对WES分析数据中微缺失/微重复结果的深度分析,并使用IGV查看相关测序数据,我们发现DYSF基因第30号外显子信号降低,可能存在单个外显子缺失。若受检者同时检出DYSF基因变异c.1**4G>T和DYSF基因第30号外显子缺失,且上述变异为复合杂合变异,则符合疾病的遗传模式,或许可以解释受检者的临床表型。我们进一步通过qPCR验证证实了受检者DYSF基因第30号外显子存在杂合缺失。当然,可能会有同行质疑qPCR的准确性,严谨地说,后续还可以进一步通过WGS和/或Sanger测序找到30号外显子缺失的精确断点。
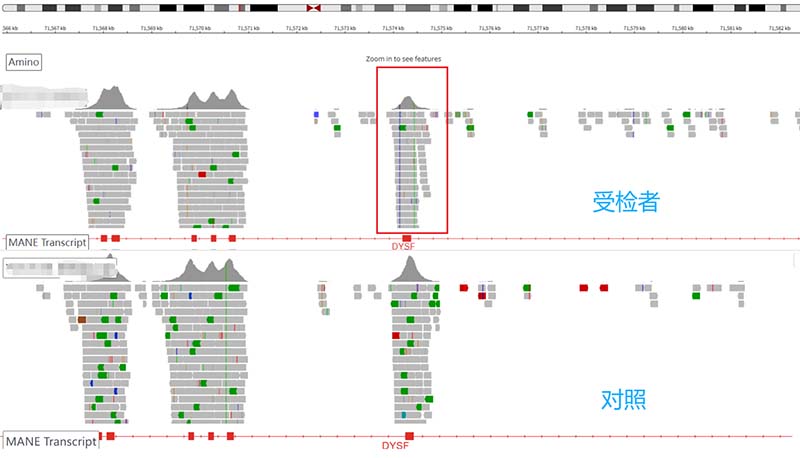
图2.WES的结果无法判断精确的断点位置,但是根据测序深度可以看到30号外显子存在缺失的可能性
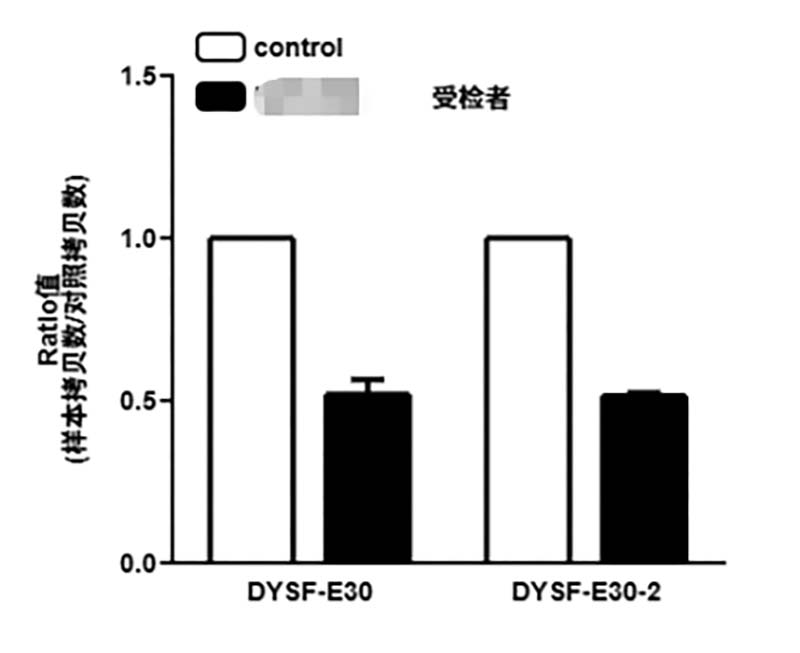
图3.qPCR验证结果提示受检者DYSF基因第30号外显子存在缺失
结果解读
评级证据(依据DYSF基因专项指南[1]):
a.PM2_Supporting:gnomAD数据库和本地数据库均未收录该变异。
b.PP3:REVEL功能预测软件结果偏向于致病性变异,预测值为0.82,预测结果仅供参考。
c.PP4:该受检者发病大于6个月且临床怀疑为LGMD,同时受检者还检出DYSF基因的另一变异。
其他相关信息:
d.疾病数据库报道:ClinVar数据库报道该变异为意义不确定变异(1颗星)。
e.文献报道:已有文献报道在1例肌病患者中检测到该杂合变异,反式相位变异未明[2]。
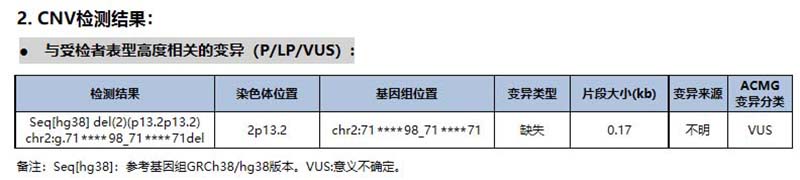
我们同时检测到DYSF基因的exon30(NM_001130987.2)的缺失。DYSF基因总共有56个外显子,在没有探明具体的断点位置时(WES的方法局限性),预计仅导致30号外显子的缺失。30号外显子是个整码外显子,且占整个基因的比例<10%。后续我们深入查询相关文献及数据库后,并未发现这个外显子涉及明确重要的功能域。
此外,人群多态性数据库DGV Gold Standard、人类基因组变异数据库ClinGen、疾病数据库Decipher等也都没有任何30号外显子缺失的记录。
结 论
到此,本次基因检测在DYSF基因中检出的变异c.1**4G>T和第30号外显子杂合缺失均为“VUS”。这似乎并不能做为临床诊断的坚实证据,还有很多的工作需要去做。
思考与总结
我们需要和临床一起找寻VUS升级的可能性。首先,受检者同时检出DYSF基因变异c.1**4G>T和DYSF基因第30号外显子杂合缺失,但是相位不明,建议受检者父母进一步验证以明确相位,这是坐实DYSF基因隐性遗传模式的首要任务。
其次,还需要对这个病人做更详细的临床分析,最好是召集MDT会议,对这个病人已经做的各项检查包括肌电图,肌肉活检等结果结合基因检测结果进行深入分析,进行针对DYSF基因相关疾病的表型-基因型分析。
最后,也给所有分子检测工作者一个警示,即当临床高度怀疑某种隐性遗传疾病,但WES仅检出其中一个杂合变异时,要进一步怀疑是否存在涉及该基因的其他变异,包括深度内含子变异、拷贝数变异、甚至是某些特殊区域的结构变异,特别是外显子水平的拷贝数缺失,这是WES的方法局限性,即便WGS也可能存在遗漏分析的风险。
参考文献
1. https://cspec.genome.network/cspec/ui/svi/doc/GN180
2. Acta Myol. 2013 Dec;32(3):148-53. [PMID:24803842]
