学术资源
产前OGM前瞻性研究成果在线发表

产前诊断是出生缺陷三级防控体系中的关键环节之一。当前,核型分析(karyotyping, KT)和染色体芯片分析(chromosomal microarray analysis, CMA)是产前遗传诊断中广泛应用的标准检测技术(standard-of-care, SOC)。这些SOC检测技术在产前遗传诊断工作中的规范应用,已经显著提升了我国出生缺陷防控工作的成效,但对另一类与出生缺陷密切相关的遗传变异,即结构变异(structural variations, SVs)的检测却始终不能得到很好的解决。
光学基因组图谱技术(optical genome mapping, OGM)在SVs检测方面已经初步显示出一定的技术优势,但未见对OGM应用于产前遗传诊断进行系统评估的报道。尤其值得注意的是,OGM对样本DNA质量要求极高,而在产前诊断临床实践中的羊水穿刺取样是否可成功进行OGM检测,更是评估OGM技术是否能够应用于产前遗传诊断的首要问题。
近日,宁波大学附属妇女儿童医院陈长水院长、李海波主任团队联合杭州金诺医学检验实验室团队完成的研究成果“Prospective Investigation of Optical Genome Mapping for Prenatal Genetic Diagnosis“在《Clinical Chemistry》杂志(IF9.3,Q1)在线发表。该研究系统评估了OGM在产前遗传诊断中的效能,并与当前产前诊断的SOC检测技术性能进行了系统比较,为后续OGM在产前诊断临床实践中的应用奠定了基础。该研究也是迄今为止全球范围内OGM技术在产前遗传诊断应用中样本量最大的一项前瞻性研究。宁波大学附属妇女儿童医院出生缺陷综合防治中心解敏为本文第一作者,杭州金诺医学检验实验室郑昭璟博士为共同第一作者,宁波大学附属妇女儿童医院院长陈长水教授、出生缺陷综合防治中心主任李海波教授、杭州金诺医学检验实验室耿娟博士为共同通讯作者。杭州金诺医学检验实验室许焱婷、任杰、方淑等参与该研究。
队列设计
此项前瞻性研究包括在宁波大学附属妇女儿童医院产前诊断中心接受羊膜穿刺术的平均胎龄为16-24周的孕妇。考虑到中国产前诊断的临床实践常规,参考了产前CMA指南、专家共识等内容来确定纳入和排除标准。纳入标准如下:(a)患有一种或多种器官异常的胎儿;(b)胎儿宫内发育迟缓>−2SD;(c)至少父母一方有染色体异常;(d)高龄产妇年龄≥35岁;(e)颈部透明层(nuchal translucency, NT)增厚(NT>3.0 mm);(f)NIPT筛查提示除T21/T18/T13外的染色体异常高风险(图1)。从2022年4月到2023年2月,共有999例需要行羊膜穿刺术的孕妇被初步考虑纳入。在应用排除标准(图1)后,共有204例病例最终被纳入研究。
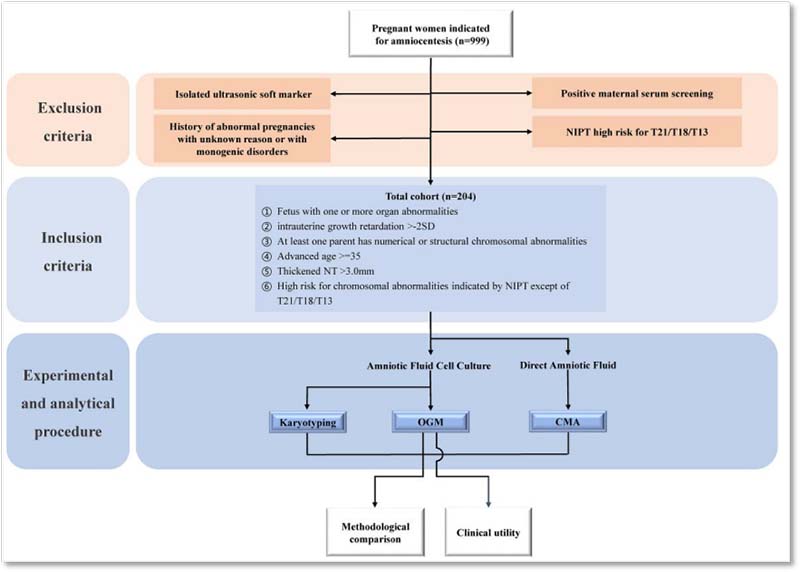
图1.队列设计流程图
根据排除和纳入标准对接受羊膜穿刺术的孕妇进行筛选。对符合条件的孕妇的羊水(AF)样本进行CMA、OGM和KT检测。
检测结果
一、技术性能
204个纳入研究的样本中,有190个样本通过了Saphyr系统数据质控,平均N50 (>150 Kb) 为281.07 Kb,比对率为91.6%,标记密度为15.73/100Kb,平均覆盖度为147.26×。OGM下机数据质控不合格率为6.8%(14/204),与CMA质控不合格率(16/204,7.8%)基本一致。由于本研究中未通过QC的样本各项质控指标仅略低于仪器制造商建议的QC阈值,因此对这些样品也进行了分析,并纳入研究结果的统计。结果表明,25%的样本细胞计数≤50万,77%的样本细胞计数≤100万。在该研究中发现,从细胞数为24万的样本中提取的DNA量足以满足正常OGM检测所需,可用于下游OGM数据分析与注释。
二、OGM和SOC检测结果的比较
研究显示,对该前瞻性队列样本单独应用OGM、CMA和KT三种检测技术进行检测,OGM的诊断率最高,OGM、CMA和KT的诊断率分别为25%(51/204)、22.06%(45/204)和18.14%(37/204)(图3B)。如果三种技术进行联合应用的话,则是OGM+KT的诊断率最高,CMA +KT次之,OGM+CMA最低,三者的诊断率分别为29.41%、28.43%和25.98%。而OGM+CMA+KT的诊断率仍为29.41%,表明这种检测策略几乎未见任何额外益处。因此整体上看,OGM+KT这两种技术联用完全可以达到OGM+CMA+KT三种技术联用的检测效能。
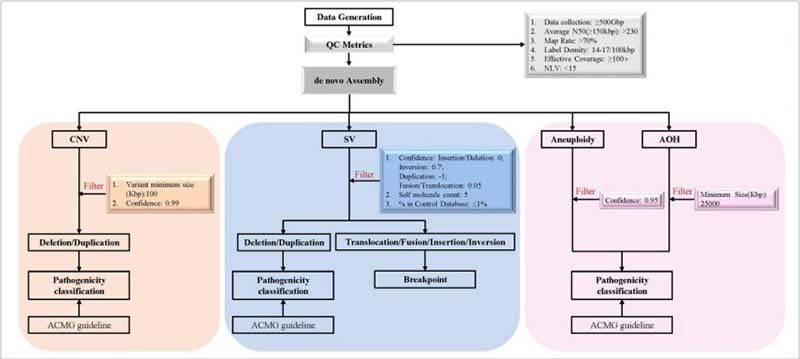
图2.OGM识别变异和数据分析的工作流程
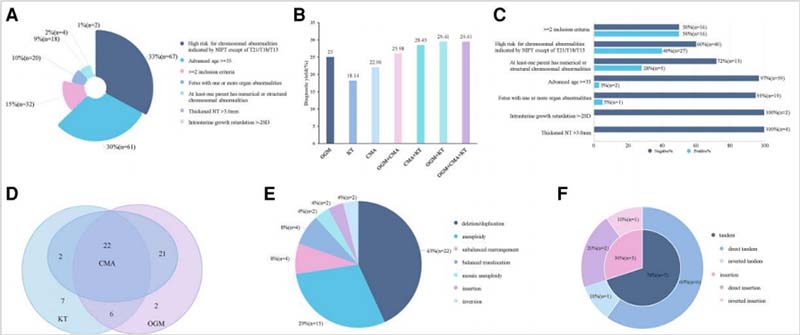
图3. 产前OGM和产前SOC检测的方法学比较
(A)所有符合条件的病例的分类;(B)OGM、KT和CMA单独或联合检测的结果;(C)每个纳入类别下阳性和阴性病例的比例;(D)OGM、CMA和KT检测的阳性病例数量的维恩图;(E)OGM的阳性结果的分类;(F)重复CNVs的方向和位置。
三、OGM和SOC检测的一致性
三种技术共鉴定出60个可报告的SVs,有22例SVs同时被三种技术检测到(图3D)。其中,OGM鉴定出51个阳性SVs,包括微缺失/微重复(n = 22,43%)、不平衡重排(n = 4,8%)、平衡易位(n = 4,8%)、非整倍体(n = 15,29%)、嵌合型非整倍体(n = 2,4%)、插入(n = 2,4%),和倒位(n=2,4%)。与CMA和KT相比,OGM在检测非整倍体、微缺失/微重复和不平衡重排方面表现出100%的一致性(表1),但仍有9例SVs被OGM漏诊。OGM与CMA的一致性为95.56%,唯一的差异是有2例嵌合型非整倍体OGM未检测到。但是CMA漏检的8个SVs均被OGM检测到,主要涉及平衡易位、插入和倒位。OGM与KT的一致性为75.68%(表1),与KT相比,OGM的分辨率更高,因此能够识别更多的不平衡重排。然而,OGM漏检的9个SVs均被KT检测到(其中7个SVs被KT单独检测到),包括着丝粒的平衡易位、低水平嵌合非整倍体、倒位、罗伯逊易位和22ps+等。总体而言,该研究结果表明,OGM针对着丝粒区、端粒区等低复杂基因组区域以及低水平嵌合SVs的检测能力仍需进一步提升。
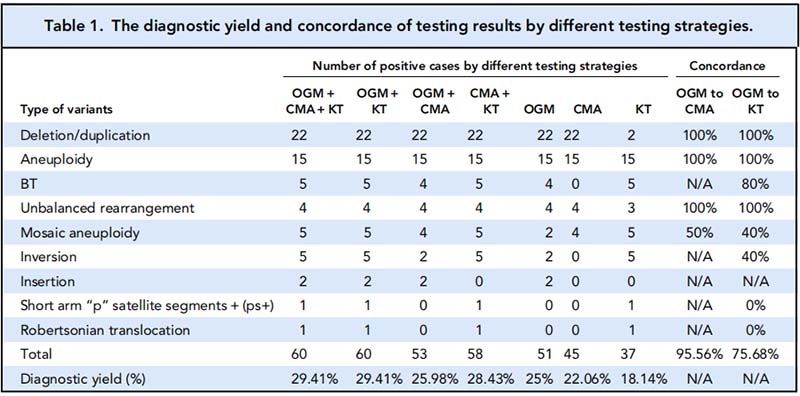
表1.不同检测技术的诊断率
四、OGM的特殊发现
①鉴定了复杂的结构重排
在C22A0861-P病例中CMA和KT显示结果正常,而OGM显示在染色体2q14.2-2q22.2区域有23.9 Mb的染色体内易位,同时在2q14.1区域有2.7 Mb的倒位(图4A)。通过长片段PCR和凝胶电泳验证了断点,并未发现基因断裂(图4B和C)。然而,这种复杂SVs的携带者在未来的生育中可能有更高的出生缺陷风险。
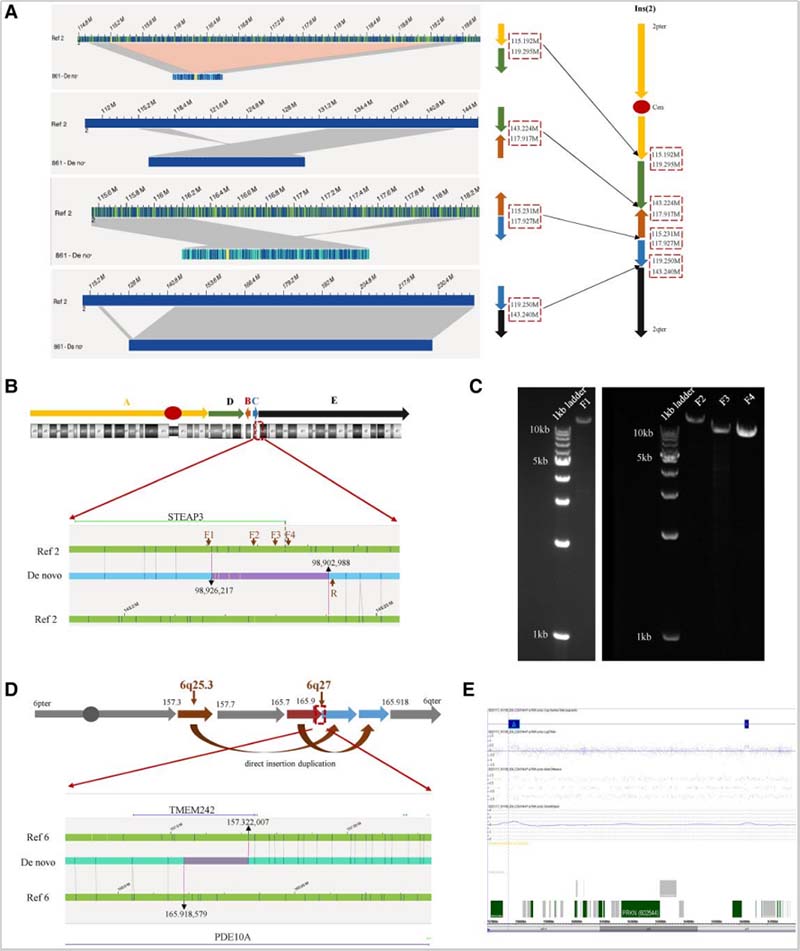
图4. 2个病例中的特殊发现
(A)病例C22A0861-P结构重排的分子图(左)和重排模型(右);(B)病例C22A0861-P致病基因的断点;(C)病例C22A0861-P长链PCR产物凝胶电泳图;(D)病例C22A1644-P的重复CNV的基因组结构;(E)病例C22A1644-P的CMA结果。
②鉴定了重复CNV的位置和方向
重复的CNVs通常通过三倍剂量产生病理效应,或有时因插入到特殊位置导致基因融合或断裂从而导致相应的功能后果。然而由于技术的局限性,SOC检测无法提供重复CNVs精确的断点和位置信息。在该项研究中,OGM对检测出的10个重复CNVs的位置和方向进行了详细的鉴定和描述,其中7个被分类为串联重复,6个病例被进一步证明为直接串联重复,第7个病例为反向重复。而其余3个插入到原来染色体的重复,1个被鉴定为反向插入,2个是正向插入(图3F)。C22A1644-P病例的KT结果正常,但CMA和OGM均检测到2个重复(图4E)。在该病例中6q25.3染色体上的一个400 Kb重复直接插入到6q27染色体区域,6q27染色体中的另一个200 Kb重复直接插入到6q25.3重复区域之后(图 4D),结果导致产生了一个融合基因TMEM242::PDE10A。因此,OGM对重复CNVs的精确断点、位置及方向信息可为此类CNV致病性判断和遗传咨询等提供重要信息。
五、随访
为了进一步揭示所报告的SVs对该队列中60例病例的临床影响,研究团队进行了短期随访。60名女性中有24名在遗传咨询后选择终止妊娠,主要是因为胎儿携带致病性SVs或超声检查异常(补充图3A和B)。其余36名孕妇还是选择继续妊娠。在撰写本文时,36名孕妇中有28名生下了健康的婴儿,而其余8名孕妇正常继续妊娠(补充图3B)。
结论
▶ 本研究尝试了培养羊水细胞的各种处理方法,初步建立了产前OGM检测羊水细胞处理的技术方案,并确定了成功进行产前OGM实验的最低细胞数量阈值(24 万)。
▶ 与KT和CMA相比,OGM的诊断率最高,初步证明了其作为产前遗传诊断临床检测技术的潜力。
▶ OGM可以提供重复CNV的详细位置和方向信息,对此类重复CNV致病性判断及遗传咨询具有较大的价值。
▶ OGM可检测KT和CMA未检测到的隐匿性染色体重排,对隐匿性染色体重排携带者的生殖规划和遗传咨询具有指导意义。
▶ 在该研究队列中,OGM+KT联合方法的诊断率与OGM+CMA+KT的方法相当。 OGM+KT技术方案可能是后续产前遗传诊断可行的路径之一,但需要更多的研究进行系统评估。
参考文献
Min Xie, Zhao-Jing Zheng, Ying Zhou, et al. Prospective Investigation of Optical Genome Mapping for Prenatal Genetic Diagnosis. Clin Chem. 2024 Mar 22:hvae031. doi: 10.1093/clinchem/hvae031. (Online ahead of print)
